Die Kjeldahl Methode zur Stickstoff- und Proteinbestimmung
Im Jahr 1883 revolutionierte Johan Kjeldahl mit seiner „Neuen Methode zur Bestimmung des Stickstoffes in organischen Körpern“ die Stickstoffanalytik und setzte neue Standards. Seither ist die Methode aus Bereichen wie der Lebensmittelanalytik, Futtermittelanalytik, Boden- oder auch Wasseranalytik nicht mehr wegzudenken. Sie beschränkt sich jedoch keinesfalls auf diese Bereiche: Auch in der allgemeinen oder pharmazeutischen Industrie und überall dort, wo der Stickstoffgehalt wichtig ist, findet man diese universell einsetzbare Methode.
Dank der vielfältigen Einsatzmöglichkeiten, der hohen Präzision und der einfachen Durchführung gilt die Kjeldahl-Analyse auch heute noch als Referenzmethode. Denn mit Hilfe der Kjeldahl-Analytik können alle Stickstoff-Komponenten erfasst werden. So können neben dem Gesamtstickstoffgehalt auch einzelne Komponenten wie Ammonium, Nitrat, Nitrit und organisch gebundener Stickstoff aus den verschiedensten Probenmatrizen ermittelt werden.
Der besondere Vorteil liegt dabei in der Vielseitigkeit der zu untersuchenden Matrizen. So können neben Getreide, Futtermitteln, Milchprodukten oder anderen Lebensmitteln beispielsweise auch Gülle, Klärschlamm, Komposte und Böden sowie wässrige Auszüge und Abwässer auf ihren Stickstoffgehalt untersucht werden. Vor allem bei stark inhomogenem Probenmaterial gibt es wegen den hohen Einwaagemengen kaum eine Alternative zu Kjeldahl.

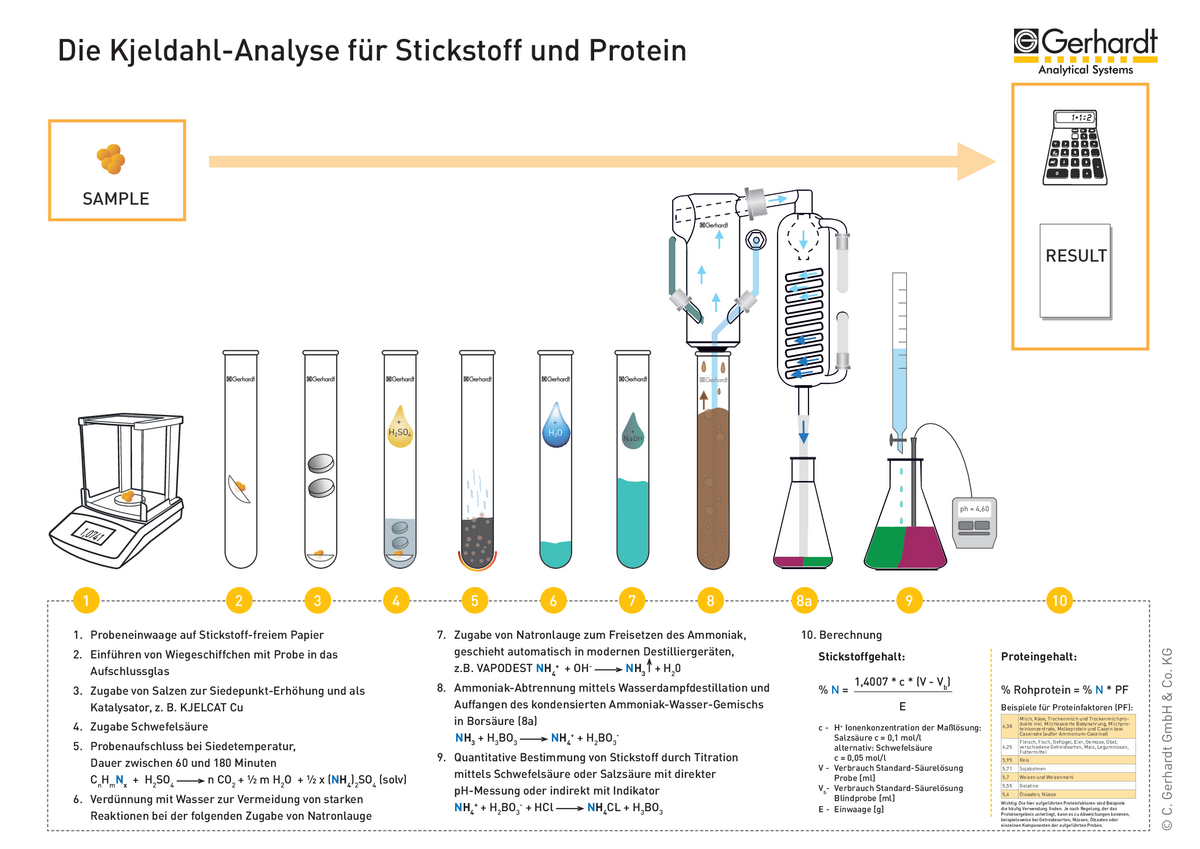
Die Kjeldahl-Analyse für Stickstoff und Protein
Bei der klassischen Anwendung kommen manuelle Laborheizer, sowie Rundkolben für Aufschluss und Erlenmeyerkolben für die Destillation zum Einsatz. C. Gerhardt hat es sich nach der Veröffentlichung der Kjeldahl-Methode zum Ziel gemacht, eben diese klassische Anwendung zu optimieren. Dafür sind im Laufe der letzten Jahrzehnte eine Vielzahl von verschiedenen Gerätetypen entstanden. Zu Beginn waren es große gusseiserne Gestelle; heute sind es hochpräzise Blockaufschlusseinheiten und Wasserdampfdestillationen mit Ergebnisberechnung und automatischer Probenzuführung.
Im Wesentlichen kann die Kjeldahl-Analyse aber auch heute noch in die 3 Arbeitsschritte unterteilt werden, die auch der klassischen Anwendung zugrunde liegen:
- Aufschluss der Proben mit Schwefelsäure
- Destillation der Aufschlusslösung mit Wasserdampf
- Titration des Destillates und Ergebnisberechnung
Die Chemie hat sich demnach nur geringfügig geändert, doch der Gesamtprozess ist mittlerweile vollständig automatisiert und an die Bedingungen von modernen Laboren angepasst. Durch die Verwendung von Aufschlussblock und Wasserdampfdestillationssystem mit integrierter Titration entstehen für den Anwender viele Vorteile.
Der Arbeitsalltag des Laborpersonals ist wesentlich sicherer, da die Präsenzzeit an den Geräten stark verringert wurde und diese mit diversen Sicherheitsfeatures ausgestattet sind. Zudem konnte der Probendurchsatz durch die automatisierten Abläufe deutlich erhöht werden. Gleichzeitig erhöht sich auch die Sicherheit der Analyse.
Für ein besseres Verständnis, wie die Kjeldahl-Analyse mit automatischen Analysensystemen abläuft, ist im Folgenden ein Schaubild aufgeführt, welches den Prozess Schritt für Schritt erklärt:
Die Automatisierung der Kjeldahl-Analyse
Total Kjeldahl Nitrogen vs. Gesamtstickstoff
Die beiden Begriffe Kjeldahl-Stickstoff (Total Kjeldahl Nitrogen, TKN) und Gesamtstickstoff (Total Nitrogen, Total N) werden oft verwechselt oder sogar für gleich empfunden, stehen aber für unterschiedliche Werte bei der Ermittlung des Stickstoffgehaltes.
Die unterschiedlichen Benennungen führen oftmals zu der Annahme, dass es sich bei TKN und Total N um zwei unterschiedliche Formen einer Stickstoffverbindung handelt. Tatsächlich beschreiben die beiden Begriffe jedoch unterschiedliche Summenparameter in der Stickstoffanalyse.
Während TKN den Anteil des gesamten gebundenen organischen Stickstoffs und Ammonium (NH4) in einer Probe beschreibt, umfasst Total N zusätzlich noch Nitrit (NO2) und Nitrat (NO3).
Der Begriff Total Kjeldahl Nitrogen (TKN) bzw. Kjeldahl-Stickstoff ergibt sich also nicht aus einer speziellen Stickstoffverbindung, sondern aus der analytischen Methode, die verwendet wurde: nämlich der Kjeldahl Methode.
Da man mit der Kjeldahl Methode neben dem Kjeldahl-Stickstoff auch den Ammonium-Stickstoff (NH4), Nitrit-Stickstoff (NO2) und Nitrat-Stickstoff (NO3) bestimmen kann, ist es möglich neben den einzelnen Stickstoffverbindungen auch die beiden Summenparameter TKN und Total N zu bestimmen. Dabei sind die unterschiedlichen Werte für verschiedene analytische Bereiche relevant:
Total Kjeldahl Nitrogen (TKN)
Der Kjeldahl-Stickstoff ist besonders im Rahmen der Abwasserbehandlung relevant, da die Bestimmung des TKN in vielen internationalen Verordnungen verpflichtend vorgeschrieben ist. Bei den einzelnen Verfahrensschritten, z.B. im Rahmen der biologischen Abwasserbehandlung, wird der Wert konstant überwacht. Dadurch kann der Gesamtprozess stets auf seine Qualität überprüft und bei Bedarf angepasst werden. Aus dem in der Probe enthaltenen Kjeldahl-Stickstoff lässt sich auch der Proteingehalt berechnen (siehe Abschnitt Protein).
Ammonium-Stickstoff
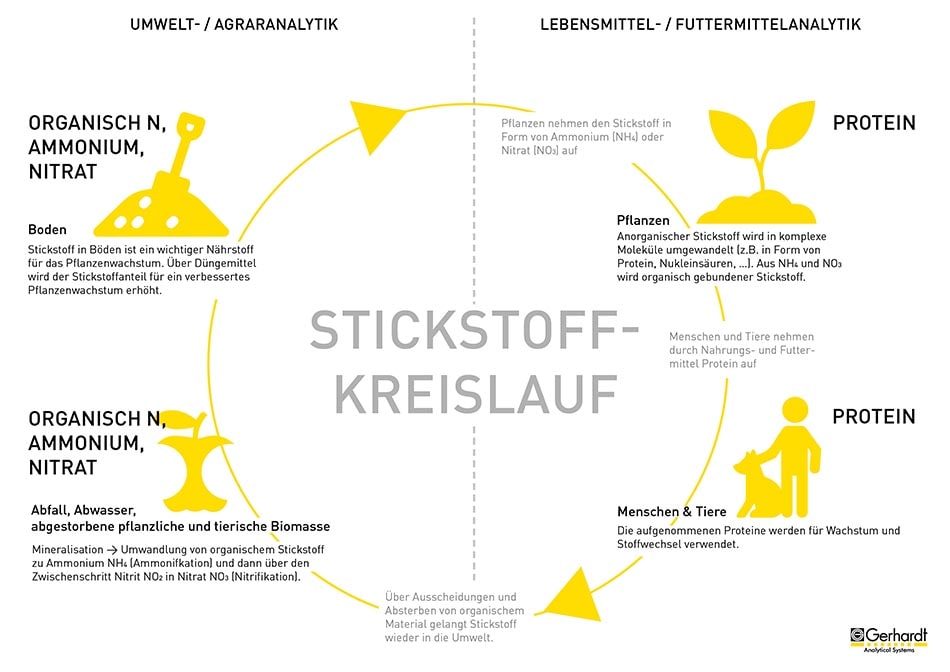
Der über Ausscheidungen und Absterben von organischem Material in die Umwelt gelangende Stickstoff liegt Anfangs vor allem in Form von organisch gebundenem Stickstoff vor. Im Rahmen der Mineralisation wird dieser im ersten Schritt in Ammonium (NH4) umgewandelt. Fachsprachlich wird dieser Prozess auch als „Ammonifikation“ bezeichnet. Anschließend wird Ammonium über den Zwischenschritt Nitrit (NO2) zu Nitrat (NO3), dies wird als Nitrifikation bezeichnet.
Die Mineralisation ist ein natürlicher Prozess der im Boden stattfindet, wenn Stickstoff aus komplexen, nicht pflanzenverfügbaren, organischen Verbindungen herausgelöst und in eine mineralische Stickstoffspezies umgewandelt wird.
Dieses Prozesses wird sich aber auch in der Umweltanalytik, beispielsweise in Klärwerken bei der Aufbereitung von Abwasser bedient, da das Wasser dadurch gereinigt wird. In Trinkwasser gibt der Ammoniumwert beispielsweise Aufschluss über den Verschmutzungsgrad des Gewässers.
Für die Landwirtschaft ist Ammonium ebenfalls relevant, da der Stickstoff in dieser Verbindung on Pflanzen aufgenommen und verarbeitet werden kann. Da es eine positive Wirkung auf das Wachstum der Pflanzen auf Äckern und Feldern hat, werden landwirtschaftliche Flächen mit Düngemitteln bearbeitet. Den Pflanzen wird dadurch schnell verfügbarer Ammoniumstickstoff zugesetzt.
Nitrat-Stickstoff
Ähnlich wie der Ammonium-Stickstoff (NH4), kann auch der Nitrat-Stickstoff (NO3) besonders gut von Pflanzen aufgenommen werden und fördert deren Wachstum. Düngemittel auf Nitratbasis werden in der modernen Landwirtschaft für eine effizientere Nutzung der vorhandenen landwirtschaftlichen Fläche genutzt.
Da Nitrat aber nur bis zu bestimmten Mengen gesundheitlich unbedenklich ist, gibt es weltweit strenge Grenzwerte für z.B. Trinkwasser. Durch eine Überdüngung landwirtschaftlicher Flächen kann überschüssiges Nitrat in Grundwasser und andere Gewässer gelangen. Deshalb muss in Gebieten mit intensiver Landwirtschaft regelmäßig die Einhaltung der Grenzwerte überprüft werden.
Protein (berechnet mit dem Proteinfaktor)
Die Bestimmung des Proteingehalts ist vor allem bei Lebens- und Futtermitteln relevant. Organisch gebundener Stickstoff (z.B. in Aminosäuren, Eiweiße, Proteine, Nukleinsäuren (DNA), …) spielt eine zentrale Rolle beim Aufbau und Stoffwechsel lebender Organismen.
Da man bei den meisten Lebensmitteln davon ausgehen kann, dass der Kjeldahl-Stickstoff hauptsächlich aus den Proteinen stammt, steht der Stickstoffgehalt einer Probe in direkten Zusammenhang mit dem Proteingehalt. Bei den meisten Proben liegt der Stickstoffanteil in den Proteinen bei 16 %, deshalb ergibt sich ein Umrechnungsfaktor von 6,25 (Stickstoffgehalt [%] * Proteinaktor = Proteingehalt [%]). Bei bestimmten Proben weicht der Anteil allerdings ab, wodurch sich ein abweichender Proteinfaktor ergibt (siehe Tabelle unten).
Proteinfaktor (Beispiele)
| Milch | 6,25 |
| Fleisch | 6,25 |
| Getreide (Ausnahme Weizen) | 6,25 |
| Weizen | 5,7 |